Le infezioni correlate all’assistenza sono una delle complicanze più gravi e frequenti dell’assistenza sanitaria e sociosanitaria. Un tempo individuate unicamente come ospedaliere o “nosocomiali”, comprendevano le infezioni insorte durante il ricovero in ospedale o dopo le dimissioni del paziente che, al momento dell’ingresso, non erano manifeste clinicamente, né in incubazione.
Negli anni l’assistenza sanitaria ha subito profondi cambiamenti e. mentre prima gli ospedali erano il luogo in cui si svolgeva la maggior parte degli interventi assistenziali, a partire dagli anni Novanta sono aumentati sia i pazienti ricoverati in ospedale in condizioni cliniche più gravi (quindi a elevato rischio di infezioni ospedaliere), sia i luoghi di cura extra-ospedalieri (residenze sanitarie assistite per anziani, assistenza domiciliare, assistenza ambulatoriale). Da qui la necessità di ampliare il concetto di infezioni ospedaliere a quello di infezioni correlate all’assistenza sanitaria e sociosanitaria.
Le infezioni correlate all’assistenza
Le infezioni correlate all’assistenza (di seguito ICA) conseguono in parte alla progressiva introduzione di nuove tecnologie sanitarie che, se da una parte garantiscono l’aumentata sopravvivenza di pazienti ad alto rischio di infezioni, dall’altra, il ricorso a procedure sempre più invasive consentono l’ingresso di microrganismi anche in sedi corporee normalmente sterili. Un altro elemento cruciale da considerare è l’emergenza di ceppi batterici resistenti agli antibiotici a causa dell’ampio e spesso inappropriato utilizzo di questi farmaci a scopo profilattico o terapeutico.
Le informazioni sulla diffusione delle ICA ad oggi disponibili confermano l’epidemiologia di decenni fa, cui si aggiunge la più moderna tendenza di alcuni patogeni a divenire maggiormente aggressivi e resistenti anche agli antibiotici di più recente generazione, proprio a causa della pressione selettiva determinata dall’abuso degli antibiotici in tutti i setting assistenziali, sia ospedalieri sia territoriali. A ciò consegue una maggiore gravità delle infezioni contratte dai pazienti ospedalizzati, che sono mediamente più anziani e più suscettibili di un tempo (ma maggiormente consapevoli dei loro diritti in tema di sicurezza delle cure), facendo rientrare la prevenzione e il controllo delle ICA nel più ampio capitolo del risk management.
La globalità del problema, dichiarata già da tempo emergenza di Sanità Pubblica dall’Organizzazione Mondiale della Sanità, viene analizzata all’interno di una recente “Review on Antimicrobial Resistance“, ricerca commissionata dal Governo Britannico e pubblicata nel 2014 dall’economista Jim O’Neill, che ha stimato come, in assenza di interventi efficaci, nel 2050 le infezioni batteriche arriveranno a causare circa 10 milioni di morti all’anno nel mondo, divenendo la prima causa di morte, riconducendoci di fatto all’era pre-antibiotica e superando ampiamente i decessi per tumore, diabete o incidenti stradali, con una perdita economica cumulativa compresa tra i 20 e i 35 miliardi di dollari.
Sebbene le evidenze scientifiche confermino la necessità di avviare processi di governo del fenomeno, ad oggi le ICA non vengono considerate un elemento di governo clinico. In particolare, per le infezioni invasive poter disporre di molecole antibiotiche efficaci è oggi più che mai importante per ridurre il rischio di esiti fatali; le elevate percentuali di resistenza registrate in alcuni Paesi europei rappresentano pertanto una seria problematica di sicurezza del paziente. L’uso prudente degli antimicrobici e le strategie di controllo delle infezioni estese a tutti i settori sanitari costituiscono i capisaldi per prevenire la selezione e la trasmissione di batteri resistenti ad agenti antimicrobici.
Punto di partenza per governare ed affrontare il fenomeno è, senza dubbio, l’attivazione di una sua sorveglianza, ovvero di sistemi di monitoraggio in grado di rilevare i casi di infezione ed i tassi di resistenza agli antibiotici da parte dei microrganismi circolanti con lo scopo di mettere in atto adeguati interventi finalizzati ad evitare ulteriori casi di infezione, limitando la trasmissione di ceppi resistenti e le occasioni di ricorso ad ulteriori terapie antibiotiche, riducendone infine i livelli di resistenza. La sorveglianza è una componente essenziale dei programmi mirati a promuovere la qualità dell’assistenza; è dimostrato in Italia, come in altri Paesi, che l’attivazione e la partecipazione a sistemi di sorveglianza attiva delle infezioni correlate all’assistenza si associa, nel tempo, alla riduzione nella frequenza delle infezioni. La disponibilità di sistemi di monitoraggio del fenomeno, di elevata qualità e accuratezza e supportati da sistemi informativi integrati, è di essenziale importanza per mantenere alto il livello di attenzione, definire le dimensioni e le caratteristiche del problema, indirizzare gli interventi, monitorarne l’efficacia ed i progressi mediante l’utilizzo di indicatori specifici ed individuare tempestivamente eventi sentinella o focolai di infezione.
Epidemiologia delle infezioni correlate all’assistenza (ICA) e dell’antimicrobico-resistenza (AMR)
La frequenza di ICA è variabile in rapporto alla tipologia di ospedale, di reparto e, soprattutto, alla complessità clinica dei pazienti trattati, anche quando si utilizzano indicatori clinici specifici. Non ha quindi senso parlare di un dato globale sulle infezioni. Attualmente, l’unico studio in letteratura che abbia stimato l’incidenza di infezioni ospedaliere a livello nazionale (inteso come indagine prospettica e rilevazione della comparsa di nuove infezioni) è lo Study on the Efficacy of Nosocomial Infection Control (Senic), condotto in un gruppo di ospedali statunitensi tra il 1975 e il 1976, che ha misurato un’incidenza di pazienti infetti e di infezioni pari al 5,2% e 6,6%, rispettivamente.
La maggior parte dei Paesi europei, compresa l’Italia, ha effettuato invece studi di prevalenza, ovvero indagini puntuali che restituiscono la “fotografia” di un fenomeno in un dato momento. La prevalenza di pazienti con ICA e la prevalenza di ICA (più infezioni possono infatti svilupparsi contemporaneamente su uno stesso paziente, con localizzazioni differenti) sono anch’esse variabili: tra il 6,8% ed il 9% dei pazienti ricoverati ha un’infezione il giorno dell’indagine e la prevalenza di infezioni è compresa tra il 7,6% ed il 10,3%. In media, quindi, sulla base di approssimazioni non applicabili a contesti specifici, si può stimare che il 5% dei pazienti ospedalizzati contragga un’infezione durante il ricovero, mentre dal 7% al 9% dei pazienti ricoverati risulti infetto in un dato momento.
In Italia non sono ancora presenti sistemi di rilevazione attiva dei dati con personale dedicato (vedi le Infection Control Nurses dei paesi anglosassoni) e quindi nel nostro Paese non esiste un sistema di sorveglianza nazionale; tuttavia, dai primi anni Ottanta, sono stati condotti numerosi studi multicentrici di prevalenza. Sulla base di questi e delle indicazioni della letteratura, si può stimare che in Italia il 5-8% dei pazienti ricoverati contragga un’infezione ospedaliera. Ogni anno, quindi, si verificano in Italia 450-700 mila infezioni in pazienti ricoverati in ospedale (soprattutto infezioni urinarie, seguite da infezioni della ferita chirurgica, polmoniti e sepsi). Di queste, si stima che circa il 30% siano potenzialmente prevenibili (135-210 mila) e che siano direttamente causa del decesso nell’1% dei casi (1350-2100 decessi prevenibili in un anno).
I dati generali sull’andamento dell’antibiotico-resistenza in Europa sono riportati ogni anno attraverso la Rete Europea di sorveglianza dell’antibiotico-resistenza EARS-Net (European Antimicrobial Resistance Surveillance Network) dell’ECDC (European Centre for Disease Prevention and Control), che coinvolge ad oggi 30 Paesi dell’UE. Nonostante il contrasto all’antibiotico-resistenza rientri ormai tra le politiche prioritarie in sanità pubblica e che siano disponibili evidenze in merito alla necessità di attivare strategie di antimicrobial stewardship e di prevenzione delle infezioni, i livelli di resistenza si mantengono elevati in molti Paesi dell’UE per numerose specie microbiche resistenti anche a più di una molecola.
L’ultimo rapporto ECDC del 2017 mostra come l’attuale situazione in Europa sia estremamente variabile in relazione al microrganismo interessato ed alla posizione geografica, questo a conferma di come alcuni Paesi si siano maggiormente impegnati per ridurre drasticamente il fenomeno, mentre per altri la situazione si mantenga ancora critica. Per quel che riguarda la sensibilità dei ceppi oggetto di sorveglianza europea (Escherichia coli, Klebsiella pneumonieae, Pseudomonas aeruginosa, Acinetobacter spp., Streptococcus pneumonieae, Staphylococcus aureus, Enterococcus faecalis, Enterococcus faecium), l’Italia si trova quasi sempre tra le ultime posizioni; ne è un esempio l’elevata percentuale di resistenza ai fluorochinoloni da parte di Escherichia coli (44,9%, il valore più elevato in tutta Europa) ed ai carbapenemi da parte di Klebsiella pneumonieae, pari a 29,7% nel 2017, valore peggiore subito dopo la Grecia (Figura 1), anche se lievemente in calo rispetto al 33,9% registrato nel 2016.
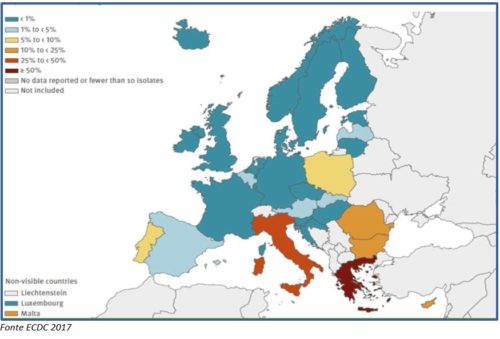
I più recenti dati ECDC confermano quindi che l’Italia è uno degli Stati membri che maggiormente si distingue per la circolazione di microrganismi multiresistenti, da attribuirsi sia all’incontrollato uso di antibiotici nel campo della salute umana ed animale, sia all’incompleta applicazione di misure efficaci per interrompere la trasmissione di infezioni.
Politiche di monitoraggio e controllo delle ICA in Liguria
Ogni Azienda Sanitaria Pubblica della Liguria si è da tempo dotata al proprio interno di un Comitato multidisciplinare per il Controllo delle Infezioni Ospedaliere (c.d. CIO Aziendali), in recepimento delle Circolari Ministeriali 52/1985 “Lotta contro le infezioni ospedaliere” e 8/1988 “Lotta contro le infezioni ospedaliere: la sorveglianza” e del successivo D.M. 13/9/1988 “Determinazione degli standards del personale ospedaliero”. Le attività di sorveglianza e controllo delle ICA in Liguria sono disciplinate da specifica normativa regionale1.
A partire dall’anno 20142è presente ed è operativo una Gruppo Tecnico Regionale per il Controllo delle Infezioni Correlate all’Assistenza, composto da esperti nel controllo del rischio infettivo in rappresentanza di tutte le Aziende Sanitarie pubbliche liguri. In collaborazione con il suddetto gruppo tecnico vengono predisposte le attività a valenza regionale per il monitoraggio ed il contenimento delle ICA e dell’antimicrobico-resistenza (AMR), più recentemente inserite negli obiettivi individuati dal più ampio Piano Nazionale di Contrasto dell’Antimicrobico-resistenza (PNCAR) 2017-2020.
La sorveglianza dell’antibiotico-resistenza in regione Liguria
A partire dal 2014 è attiva in Liguria la sorveglianza dell’AMR a partire dai dati di routine dei laboratori pubblici di microbiologia. A differenza dei network europeo e nazionale che raccolgono informazioni sulle sole infezioni invasive (percentuale di resistenza di microrganismi isolati su sangue e liquor), il network regionale si basa sulla identificazione di ceppi resistenti di microrganismi isolati da qualsiasi campione biologico proveniente da tre possibili setting assistenziali (degenza ospedaliera, lungodegenza/RSA, esterni/ambulatoriali), che corrisponde a circa 80.000 microrganismi isolati ogni singolo anno di analisi.
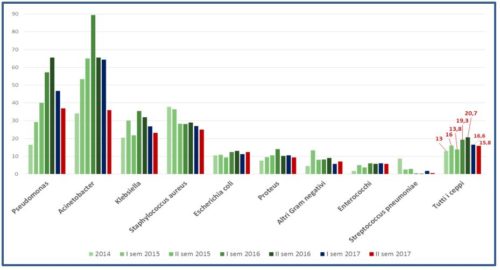
I dati dell’ultimo periodo di analisi (1 luglio-31 dicembre 2017) sono relativi a 42.325 microrganismi, di cui 4.730 (11,2%) isolati da siti sterili (sangue o liquor). Rispetto ai periodi precedenti, si osserva in Liguria un trend in lieve riduzione per quel che riguarda la resistenza nei confronti dei carbapenemici da parte di Klebsiella pneumoniae (dal 16% circa del 2016 all’attuale 10%). Nel corso degli anni di osservazione (Grafico 1), si è inoltre registrata una netta riduzione della percentuale di Staphylococcus aureus meticillino-resistente (Methicillin-Resistant Staphylococcus Aureus – MRSA), che è passata dal 38% del 2014, al 25% del II semestre 2017, ben al di sotto della media nazionale (33,9%), avvicinandoci maggiormente alla media dei Paesi dell’UE (circa 20% di MRSA).
Lo screening dei portatori di enterobatteri produttori di carbapenemasi ricoverati in strutture sanitarie e sociosanitarie
La sorveglianza attiva e il riconoscimento precoce di tutti i soggetti colonizzati da enterobatteri produttori di carbapenemasi (CPE), che rappresentano potenziali serbatoi e fonti di diffusione, il loro isolamento e la messa in atto di tutte le precauzioni aggiuntive “da contatto”, ha l’obiettivo sia di ridurre la circolazione “invisibile” di questi microrganismi, sia di evitare la trasmissione ad altri pazienti con condizioni predisponenti a quadri clinici più severi. Con la D.G.R. 529 del 27/03/2015 è stato approvato il Protocollo Regionale “Gestione di Enterobacteriaceae resistenti ai carbapenemi nelle strutture sanitarie”, specifico atto di indirizzo alle Aziende Sanitarie Pubbliche della nostra Regione. Le indicazioni in esso contenute comprendono tutte le misure precauzionali atte ad impedire o contenere la trasmissione da soggetti infetti o colonizzati, tra queste, l’identificazione tempestiva e l’isolamento dei pazienti colonizzati/infetti per coorte o in stanza singola, l’adozione da parte del personale delle precauzioni da contatto, ecc.
Lo stesso protocollo ha previsto l’attivazione di una sorveglianza attiva mirata alla individuazione precoce dei soggetti colonizzati da CPE ricoverati presso strutture sanitarie pubbliche, ossia l’effettuazione di un test di screening all’ingresso (tramite tampone rettale) in tutti i soggetti ricoverati che, per tipologia di reparto di degenza o per caratteristiche individuali, presentano un maggior rischio di colonizzazione al momento del ricovero. Nell’arco temporale di tre anni (2015-2017), sono stati sottoposti a screening circa 94.363 pazienti negli ospedali pubblici e nelle RSA pubbliche e private accreditate; complessivamente, l’8,4% dei pazienti sottoposti a screening è risultato essere portatore di un CPE (nel 98% dei casi è stata isolata Klebsiella pneumoniae) con percentuali di positività più elevate all’interno delle strutture residenziali (11,4%) rispetto agli ospedali per acuti (6,3%).
Sorveglianza delle batteriemie da CPE in Liguria
La Circolare Ministeriale n. 4968 del 26/02/2013 ha istituito la Sorveglianza nazionale delle batteriemie da Klebsiella pneumonieae ed Escherichia coli produttori di carbapenemasi, inserendole di fatto tra le malattie soggette a notifica obbligatoria. La Liguria ha da subito recepito le indicazioni ministeriali , il flusso informativo è a regime dal 2015 e l’andamento delle notifiche dei casi viene quindi attentamente monitorato a livello regionale.
Come è evidente anche dall’ultimo Rapporto redatto dall’Istituto Superiore di Sanità, trattandosi di un flusso basato su segnalazione volontaria dei casi osservati, la conseguenza naturale è che proprio le regioni tradizionalmente più virtuose e più attive nel contrasto alle ICA e all’AMR siano quelle che registrano valori più elevati; le frequenze assolute osservate sono pertanto influenzate dal livello di attenzione delle singole regioni e non rispecchiano evidentemente la reale distribuzione del fenomeno. I dati liguri riportati nel Grafico 2 corrispondono a tutti i casi di batteriemie sostenute da CPE, che, a partire dal 2013, vengono segnalati di routine al centro di riferimento regionale (attuale S.C. Prevenzione di A.Li.Sa.) e all’Istituto Superiore di Sanità.
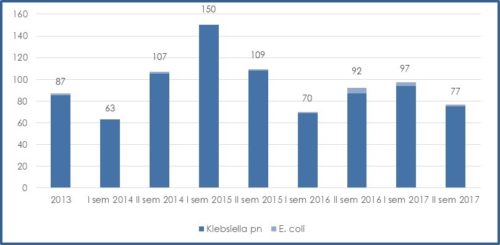
I dati regionali a nostra disposizione, a fronte della consistente numerosità in termini assoluti, possono essere positivamente interpretati quale espressione di un progressivo aumento di sensibilità nella segnalazione dei casi da parte degli operatori liguri; gli stessi numeri assoluti, quando confrontati con il totale degli esami colturali effettuati in Liguria (espressi quindi come percentuale di batteriemie sostenute da CPE sul totale delle emocolture), mostrano in realtà un trend in riduzione a partire dall’anno 2015 (Grafico 3). Tale decremento appare coincidere temporalmente proprio con l’approvazione ed adozione in Liguria3 del Protocollo Regionale “Gestione di Enterobacteriaceae resistenti ai carbapenemi nelle strutture sanitarie”, potenziale espressione di una aumentata sensibilità e di una migliorata capacità di gestione della problematica.

Indagini annuali di prevalenza delle ICA e del consumo di antibiotici negli ospedali per acuti
Oltre ad aver preso parte, nel 2016, alla realizzazione di uno studio di prevalenza Europeo sulle infezioni correlate all’assistenza e sull’utilizzo di antibiotici negli ospedali per acuti promosso dall’ECDC, la Regione Liguria ha inserito, tra gli obiettivi del proprio Piano Regionale della Prevenzione 2014-2019, l’effettuazione di un’indagine regionale di prevalenza che coinvolge ogni anno (rilevazione nel periodo marzo-aprile) tutti gli ospedali pubblici della Liguria, utilizzando il medesimo protocollo di studio proposto dall’ECDC. Trattandosi di uno studio di prevalenza puntuale, questo ci permette di rilevare quante infezioni sono presenti, in un dato momento, in tutti i pazienti ricoverati in ospedale il giorno dello studio.
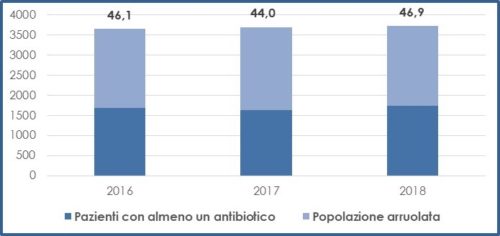
I risultati della prima analisi condotta nel 2016 sono stati oggetto di pubblicazione su rivista scientifica internazionale [4] ed attualmente disponiamo dei dati raccolti negli anni 2016, 2017 e 2018. Appare utile analizzarne complessivamente i risultati e seguirne l’andamento temporale, sia per rilevare le possibili criticità esistenti, ovvero verificare eventuali effetti di miglioramento quale risultato delle attività di contrasto alle ICA e all’AMR da tempo poste in essere nella nostra Regione. Entrambi i fenomeni indagati non hanno subito variazioni significative negli ultimi tre anni, né la frequenza di ICA diagnosticate, né tantomeno la quantità di antibiotici utilizzati (Grafico 4 e 5). Il dato nazionale di riferimento (8,03%) non è direttamente confrontabile con il nostro dato regionale, in quanto misurato nel più ampio contesto della precedentemente citata indagine europea, che prevedeva l’adesione volontaria di pochi ospedali partecipanti per ciascuna regione (presumibilmente già maggiormente sensibili ed attenti alla problematica) e non invece un arruolamento estensivo di tutti gli ospedali presenti sul territorio come in Liguria.
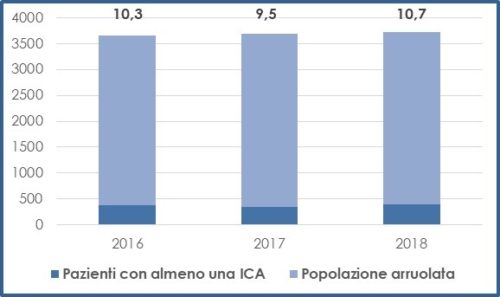
Sebbene con valori differenti tra Aziende liguri, in relazione soprattutto alla variabilità nel case-mix dei pazienti trattati, mediamente in Liguria un paziente su 10 presenta almeno una ICA il giorno della rilevazione. Dall’ultima rilevazione regionale del 2018, le localizzazioni di infezione più frequenti erano le polmoniti e le infezioni del tratto urinario (frequenza relativa 19% e 19,2%, rispettivamente), seguite dalle infezioni del sangue (16,7%) e le infezioni del sito chirurgico (11,7%).
Per quanto riguarda il consumo di antibiotici rilevato nel corso dell’indagine del 2018, 5.046 pazienti (45,7%) erano in trattamento antibiotico per via sistemica (78% per via parenterale e 22% per via orale) il giorno dello studio, per un totale di 6.943 antibiotici prescritti (con una media di 1,4 antibiotici per paziente).
La prevalenza di pazienti in trattamento antibiotico variava dal 4,2% in psichiatria al 59,9% in terapia intensiva. Rilevante l’utilizzo in chirurgia, dove il 50,7% dei pazienti stava assumendo almeno un antibiotico. L’indicazione al trattamento era nel 71,2% il trattamento di un’infezione, nel 29% dei casi una profilassi (56,7% medica, 43,3% chirurgica). Anche per quel che riguarda l’appropriatezza nella prescrizione antibiotica, questa risultava ancora carente per molti aspetti in termini di indicazione, di scelta della molecola, dosaggio e tempi di somministrazione.
Seppur tali informazioni non fossero sempre registrate in cartella clinica (motivazione alla prescrizione assente nel 20-30% dei casi), l’indicazione ed i tempi di somministrazione dell’antibiotico risultavano spesso incongruenti; potrebbe rappresentare un esempio di utilizzo inappropriato il dato relativo alla somministrazione dell’antimicrobico in profilassi chirurgica per più di un giorno nel 49,4% dei pazienti, in quanto non sussistono, nella maggior parte dei casi, evidenze che documentino come il prolungamento della profilassi chirurgica per un periodo superiore alle 24 ore riduca il rischio infettivo; vi sono al contrario segnalazioni di un’aumentata incidenza di coliti da Clostridium difficile e, addirittura, di un maggior numero di infezioni sostenute da batteri resistenti all’antibiotico impiegato.
La necessità di prolungare la somministrazione di una molecola antibiotica dovrebbe essere riportato in cartella clinica e, qualora si sospetti l’insorgenza di una problematica infettiva, il farmaco utilizzato, questa volta come terapia, dovrebbe essere una molecola diversa da quella utilizzata in profilassi, eventualmente allargando lo spettro antimicrobico. L’ampio utilizzo di molecole in profilassi chirurgica per periodi superiori alle 24 ore potrebbe pertanto essere inquadrato come rappresentativo di quest’ultima evenienza.
Conclusioni
Sebbene negli ultimi anni siano stati compiuti progressi significativi nell’attuazione delle strategie di prevenzione negli ospedali liguri, le ICA continuano a rappresentare un serio problema di salute pubblica, anche nella nostra Regione. L’alta prevalenza di infezioni, specialmente nelle unità di terapia intensiva, necessita sia di una continua sorveglianza delle ICA sia di politiche efficaci per contenere i focolai, attraverso una piena comprensione della tipologia di infezioni e delle popolazioni di pazienti colpite. Gli alti tassi di resistenza ai carbapenemi e l’elevato ricorso all’uso di antimicrobici, spesso ingiustificato, illustrano l’urgente necessità di implementare un uso più razionale degli stessi e di rafforzare ulteriormente il controllo delle infezioni a livello regionale e locale.
Gli studi di prevalenza puntuale annualmente ripetuti e gli altri flussi informativi di cui attualmente disponiamo in Liguria, forniscono una grande quantità di informazioni sulla dimensione del fenomeno e sul suo andamento nel tempo, evidenziando i potenziali effetti delle strategie adottate. La restituzione dei dati, raccolti ed elaborati, contribuisce a promuovere una maggiore attenzione al problema e a rafforzare infrastrutture e competenze; inoltre l’individuazione di problemi comuni consente di stabilire priorità condivise, di valutare l’impatto delle strategie e di affrontare le scelte politiche locali.
Note
- DGR 1702/2014 – Approvazione Piano Regionale della Prevenzione-, DGR 730/2015 – Sviluppo PRP-, DGR 10/2016 – Integrazioni e modifiche PRP, DGR 529/2015 – Approvazione di direttiva vincolante ai sensi dell’art.8, comma 1 della L.R. 41/2006 e ss.mm.ii. in materia di procedure di prevenzione e di controllo delle infezioni ospedaliere
- Determina del Direttore Generale di ARS Liguria n. 58 del 19/05/2014 e ss.mm.ii. e Deliberazione di A.Li.Sa. n. 97 del 28/03/2019
- DGR Regione Liguria 529 del 27/03/2015
Bibliografia
O’Neill J., (2016), Tackling Drug-Resistant Infections Globally: Final Report in The Review on Antimicrobial Resistance chaired, May
Antimicrobial resistance surveillance in Europe, 2017, ecdc eu
Sabbatucci M., Iacchini S., Iannazzo S., Farfusola C., Marella A. M., Bizzotti V., D’Ancona F., Pezzotti P., Pantosti A., (2017), Sorveglianza nazionale delle batteriemie da enterobatteri produttori di carbapenemasi. Rapporto 2013-2016, Rapporti ISTISAN – luglio, 3° Suppl.
Sticchi C., Alberti M., Artioli S., Assensi M., Baldelli I., Battistini A., Boni S., Cassola G., Castagnola E., Cattaneo M., Cenderello N., Cristina M.L., De Mite A.M., Fabbri P., Federa F., Giacobbe D.R., La Masa D., Lorusso C., Marioni K., Masi V.M., Mentore B., Montoro S., Orsi A., Raiteri D., Riente R., Samengo I., Viscoli C., Carloni R., (2018), The Collaborative Group for the Point Prevalence Survey of healthcare-associated infections in Liguria. Regional point prevalence study of healthcare-associated infections and antimicrobial use in acute care hospitals in Liguria, Italy in Journal of Hospital Infection, 99:8-16













