La presa in carico della persona con Disturbo Cognitivo Soggettivo (SCD) e Disturbo Neurocognitivo lieve (MCI)
Negli ultimi venti anni molte cose sono cambiate nell’ambito dei servizi per le demenze, ma l’importanza del ‘prendersi cura’ dell’altro resta un tema di centrale importanza. La presa in carico richiede attenzione in ogni fase della malattia, ma diviene azione di estrema complessità soprattutto nelle situazioni borderline. Questo ci richiama alla necessità di cooperazione e di riconoscere il fondamentale ruolo di tutti gli attori della cura per garantire una reale presa in carico dei bisogni contingenti della persona.
19 Dicembre 2019
Numero 5-2019
di Federica Gottardi (psicologa-psicoterapeuta Fondazione I.P.S. Cardinal Gusmini Onlus di Vertova) Elena Lucchi (psicologa presso la Fondazione Teresa Camplani Casa di Cura “Ancelle della Carità” di Cremona)
Sono passati quasi 20 anni dall’avvio del Progetto Cronos e la nascita delle Unità di Valutazione Alzheimer per la diagnosi e la cura delle demenze. Molte cose oggi sono cambiate, in primis le aspettative nei confronti di quest’ultima, della cura. Ciò che in questi anni forse non è cambiato, nonostante i progressi della comunità scientifica e l’avanzare delle conoscenze sulle caratteristiche delle patologie neurodegenerative, è la consapevolezza che il prendersi cura della persona, il to care, rappresenta ancora e sempre l’intervento fondamentale nella battaglia contro la demenza.
La Persona al centro
Il concetto latino persona, così come l’analogo concetto greco prosopon, appartiene al mondo teatrale e significa ‘la parte distinta da colui che la recita’, interprete vs personaggio. Persona era la maschera attraverso la quale risuonava la voce dell’attore; successivamente questo termine è stato associato anche, in senso figurato, al suo ruolo nella società, lo status sociale. L’etimologia latina di persona fa riferimento alla maschera dell’attore teatrale che per-sonat, e cioè “parla attraverso”, risuona, mentre l’etimologia greca di prosopon fa riferimento alla maschera, ma allude a quello che si vede di qualcuno che sia davanti a noi, e che è pros-opsis, e cioè “davanti al nostro sguardo”. Cosi si apre il saggio La dignità ferita di Eugenio Borgna (2013). L’etimologia del termine persona concede dunque molteplici riflessioni in merito al tema della considerazione, del rispetto e soprattutto della cura; una cura volta principalmente al riconoscimento dei bisogni e, in primis, della dignità della persona stessa che si trova in una condizione di disabilità (fisica, psichica e/o cognitiva).
“Sono trascorsi molti secoli prima che si giungesse a riconoscere alla persona umana valori universali” ha scritto Robert Spaemann, uno dei grandi filosofi contemporanei. Borgna, nel suo saggio del 2013 “La dignità ferita”, si chiede quale qualità qualcuno debba possedere per avere il diritto di essere riconosciuto come persona, e risponde attraverso le parole del filoso tedesco dicendo che “quando ‘qualcosa’ è ‘qualcuno’, egli è, e non può se non essere, persona”. La riflessione fenomenologica sottende l’idea che essere qualcuno non è una qualità dell’essere vivente, ma la qualità di una persona con la sua libertà e la sua dignità. Nel mondo antico è stato Cicerone a riflettere circa il problema della dignità umana e a sostenere che l’uomo si differenzia dagli altri uomini per il ruolo significativo che egli svolge nella vita pubblica. La dignità gli viene dalla sua posizione nella scala gerarchica sociale e le attribuisce un valore relativo: la si può avere e la si può perdere.
Tutti gli uomini sono dunque persone e fanno parte fino alla morte della comunità delle persone, della società. Di questa comunità fanno parte anche coloro che sviluppano una malattia, con disturbi psichici e/o fisici, e che a causa di tale condizione perdano, o temano di perdere, la capacità di autonomia. Su questa considerazione si fonda il principale conflitto interno ai servizi di cura per anziani ai quali afferiscono persone con disturbi cognitivi, soggettivamente percepiti, riferiti, o oggettivamente riscontrati. Nella realtà dei servizi di cura per anziani collochiamo, tra i sopracitati, i quadri borderline in cui si osserva un deterioramento cognitivo che non soddisfa però i criteri per la diagnosi di demenza poiché tali difficoltà non impattano in modo significativo sull’indipendenza della persona, mantenendola così nello status di persona secondo la definizione di Cicerone.
Difficoltà cognitive e Persona: la presa in carico
Le persone che si trovano in questo territorio di mezzo sono meritevoli di particolare attenzione, non solo perché potrebbero beneficiare di un trattamento immediato e diretto, ma anche perché i disturbi riferiti o riscontrati potrebbero rappresentare un indice precoce di malattia neurodegenerativa. I concetti di Subjective Cognitive Disorder (SCD) e di Mild Cognitive Impairment (MCI) sono stati introdotti per meglio definire, e per differenziare, questa fase di transizione tra l’invecchiamento normale e quadri patologici (Petersen et. al., 1999) (Tabella 1).
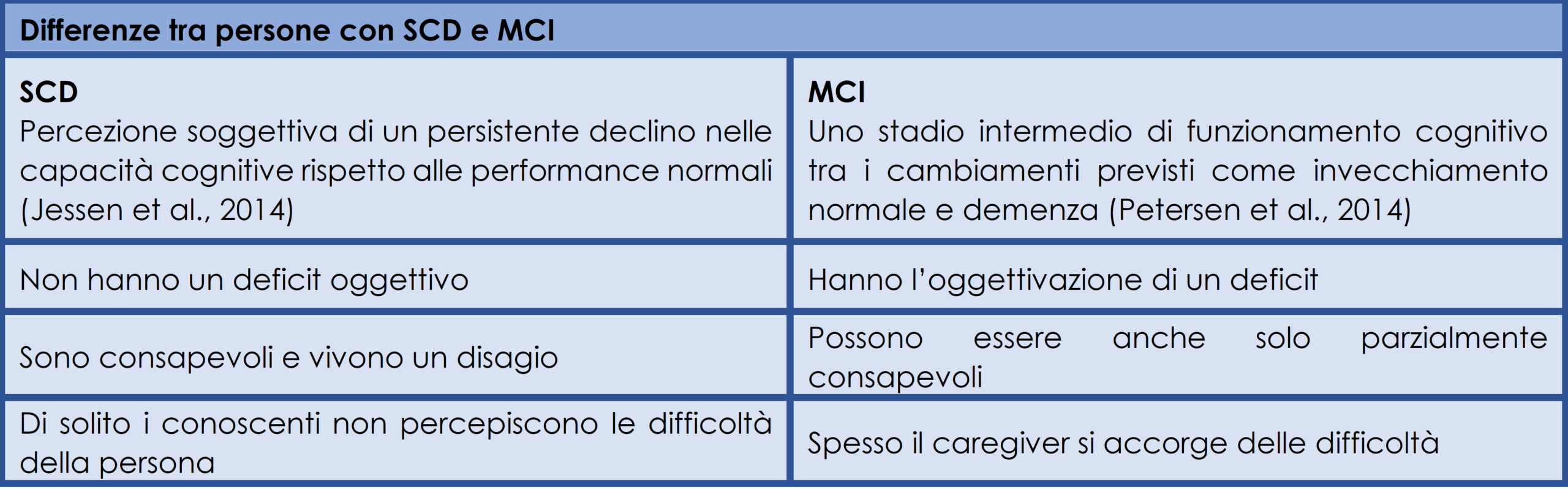
Tabella 1 – Differenze tra persone con Subjective Cognitive Decline (SCD) e Mild Cognitive Impairment (MCI)
È ormai consolidato in letteratura il legame tra MCI e demenza, con dati a supporto del maggiore rischio di sviluppare demenza per le persone con MCI (Petersen et al., 1999 e 2018). Altri importanti contributi scientifici ci informano inoltre circa la probabilità di sviluppare demenza, che pare essere quasi il doppio rispetto ai soggetti normali, anche per le persone con SCD (Mitchell et al., 2014). Questi dati ci obbligano ad una riflessione: se è vero che l’identificazione di un MCI o di un SCD può essere associato a sentimenti positivi in quanto esclude, anche se probabilmente solo per il momento, il timore di ricevere una diagnosi peggiore, qual è quella di demenza, è pur vero che risulta di fondamentale importanza non abbandonare, ma accompagnare le persone che ricevono una diagnosi di MCI o SCD.
Le raccomandazioni consigliate per la gestione della persona con MCI, seppur con diversi livelli di evidenza, oltre a includere la valutazione dei fattori di rischio modificabili, dello stato funzionale e dei sintomi psicologici e comportamentali, il monitoraggio dello stato cognitivo nel tempo, lo svolgimento di un regolare esercizio fisico e allenamento cognitivo, prendono in considerazione la possibilità di affrontare gli aspetti della diagnosi, la prognosi, la pianificazione a lungo termine (Petersen et al., 2018). Emerge quindi come centrale la presa in carico psicologica che possa supportare e accompagnare il disagio psichico conseguente alla percezione di un cambiamento nel proprio funzionamento cognitivo e alla condizione di rischio di sviluppare in futuro una demenza.
Dietro alla diagnosi di MCI o di SCD si nasconde una persona che vive, nel momento della consultazione, un disagio che deve essere accolto e accompagnato, non semplicemente monitorato nel tempo o sbrigativamente rassicurato con uno “Stia tranquillo, lei non ha nulla di grave o di importante”. Tanto quanto è necessaria la rilevazione della possibilità che i sintomi celino una condizione preclinica di malattia, non va trascurata la frequente reazione di distress psicologico ed emotivo provato da queste persone. Percepire un cambiamento nelle proprie prestazioni cognitive può elicitare reazioni e sentimenti di rabbia e paura. Tantomeno non dobbiamo dimenticare l’evidenza di disturbi d’ansia e dell’umore quali sintomi comuni in persone che ricevono diagnosi di SCD e MCI (si veda la revisione di Bhome et al., 2018). È pertanto dovere etico dei professionisti della cura dare una spiegazione e una risposta al cambiamento percepito dalla persona. Va accolta e giustificata la reazione di distress e va indirizzata la persona verso un percorso che dovrebbe avere l’obiettivo di favorire l’adattamento alla nuova condizione; status che rappresenta un peggioramento rispetto alle sue aspettative o a una situazione pregressa. Accompagnare all’adattamento significa rimodulare la distanza tra realtà e aspettative, ottenendo come risultato un miglioramento della qualità di vita della persona (si veda il concetto di “Calman’s gap”1).
Per quanto riguarda le persone con SCD la situazione è però ancora più variabile rispetto agli MCI:
- meno del 20% dei pazienti anziani che considerano la propria memoria compromessa hanno consultato un medico (Waldorff et al., 2008);
- tra i soggetti che riferiscono disturbi di memoria con impatto sulla vita quotidiana, solo il 26% aveva consultato un medico (Begum et al, 2012);
- tra diciassette sintomi diversi come angina, asma, problemi di udito, mal di testa, insonnia, eccetera, il disturbo di memoria soggettivo è il quinto in termini di prevalenza, ma quello che con minore probabilità porterà ad un consulto medico (Begum et al., 2012).
La prevalenza del SCD tra le persone che afferiscono ai servizi per la valutazione dei disturbi di memoria è molto elevata e variabile: dal 18% al 55% (si veda la revisione di Bhome et al., 2018). Non c’è tuttavia un accordo in merito alla gestione delle persone con SCD e, fino ad ora, i centri per i disturbi di memoria tendono a privilegiare il trattamento delle persone con deficit cognitivi dovuti a malattie definite. Anche se, come riportato sopra, le persone con SCD hanno un elevato rischio di sviluppare demenza, tuttavia solo il 14% delle persone con SCD evolve in MCI o Malattia di Alzheimer (AD) a 6 anni (Hessen et al., 2017). Frequentemente infatti i sintomi sembrano andare in remissione.
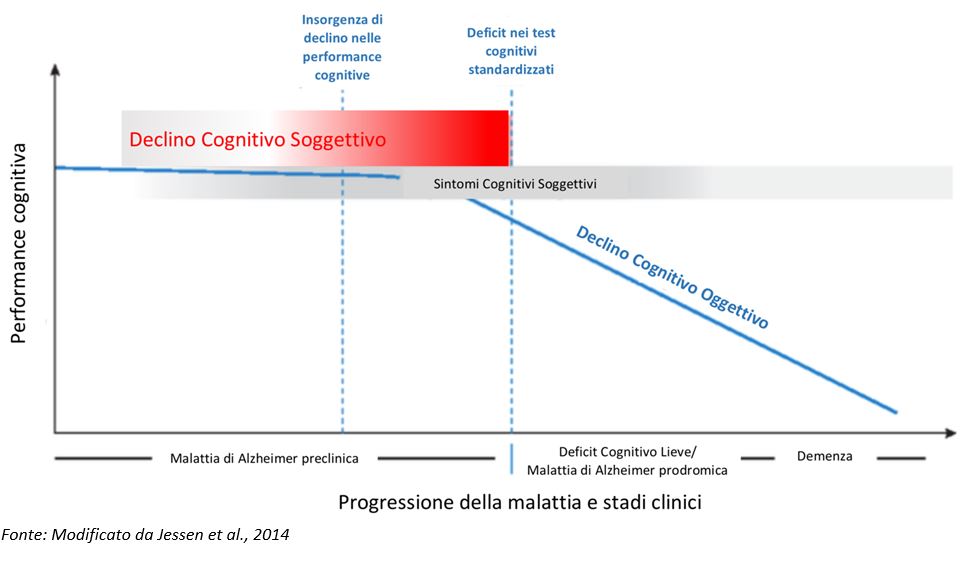
Figura 1 – Declino Cognitivo Soggettivo (Subjective Cognitive Decline -SCD) proposto come possibile stadio preclinico della Malattia di Alzheimer
Poiché le indagini strumentali che potrebbero distinguere tra SCD preclinico AD vs non-preclinico non sono attualmente usate in modo routinario, l’approccio al problema della gestione delle persone con SCD consiste prevalentemente in un regolare monitoraggio negli anni, spesso senza offrire altri tipo di intervento specifico. Con sempre maggiore frequenza i Centri per i Disturbi Cognitivi e Demenza (CDCD) e i servizi per le demenze vengono a contatto e si devono confrontare con i peculiari bisogni di cura che queste persone portano. Come avviene oggi la presa in carico di queste persone all’interno dei servizi per le demenze?
Purtroppo, l’attuale assetto normativo prende in considerazione solo limitatamente una delineazione di specifici percorsi di presa in carico delle persone con SCD e MCI, sebbene oggi si ritenga tale condizione di frequente riscontro nell’ambito delle richieste di valutazione al CDCD. Inoltre, attualmente si osserva nelle diverse realtà territoriali una spinta all’implementazione di proposte o raccomandazioni finalizzate ad una diagnosi tempestiva che individui i soggetti a maggior rischio di sviluppo di demenza dovuta a Malattia di Alzheimer (Progetto RELOAD – Progetto Rete Lombardia Orientale per la diagnosi precoce della Malattia di Alzheimer e Declino Cognitivo).
Allo stesso modo, al CDCD non è attribuito solo un ruolo diagnostico ma più ampiamente una responsabilità di presa in carico nel cui contesto appaiono altrettanto fondamentali la comunicazione della diagnosi, la consulenza e il supporto psicologico, eventuali trattamenti farmacologici e non farmacologici, il management degli stili di vita, le certificazioni medico-legali. Un esempio positivo si trova nel documento “Indicazioni per I servizi della rete nella cura delle persone con demenza ed il sostegno ai familiari Regione Emilia-Romagna” (D.G.R. 2581/99) del 2016, dove vengono specificate le indicazioni operative da attuare in caso di presenza di deficit cognitivo lieve, in assenza di demenza (MCI come condizione di rischio): “Il centro per i disturbi cognitivi dovrà concordare un appuntamento di follow-up a 12 mesi e comunque informare il MMG sull’esito della visita. In presenza di tale condizione, è inoltre necessario informare il paziente circa i corretti stili di vita da adottare, in quanto il MCI rappresenta appunto una condizione di maggiore rischio”. Non vengono tuttavia date indicazioni in merito alla possibilità di offrire ulteriori interventi specifici per queste persone e non uno sguardo alle condizioni di SCD.
Nelle Linee di indirizzo Nazionali sui Percorsi Diagnostico Terapeutici Assistenziali per le demenze (2017) viene sottolineato come la presa in carico della persona e della sua famiglia sia un compito dell’équipe di cura che, in accordo con gli interessati, identifica l’intervento migliore. La prospettiva della presa in carico è attiva e totale, dalla prevenzione alla riabilitazione fino alle cure palliative e di fine vita, sottolineando la necessità di interventi multiprofessionali e multidisciplinari attuati in diversi ambiti tra cui quello psico-fisico, sociale e delle eventuali disabilità. La cura della demenza, e delle fasi che la precedono, è un intervento complesso che deve poter contare sulla molteplicità delle figure professionali coinvolte, sia nella fase di valutazione e di indagine diagnostica che di impostazione del piano terapeutico che deve delineare il percorso di presa in carico totale.
Una presa in carico complessa che vede nel ruolo di co-protagonista, riprendendo la metafora teatrale di apertura, il familiare. Spesso una voce solista, talvolta un coro, ma un attore che ha in sé la sofferenza legata al cambiamento e all’incertezza ma anche l’opportunità di essere risorsa. La drammatica certezza moderna è che al senso di isolamento e di solitudine che spesso vivono le persone con decadimento cognitivo e le loro famiglie spesso si accompagna un senso di disorientamento rispetto alla rete dei servizi territoriali e alle opportunità di supporto.
Quali interventi?
Come sottolineato pocanzi, tema centrale della presa in carico negli ultimi anni, e fondamento dei molteplici interventi psicosociali di prevenzione del disagio e di promozione della salute, sono i bisogni della famiglia. Tuttavia, le persone che vivono una condizione di SCD o di MCI esprimono bisogni complessi. Esse devono divenire protagoniste del percorso di cura, devono essere incluse attraverso la promozione di opportunità. Seppur non esista un consenso sui trattamenti non farmacologici statisticamente efficaci con persone con SCD, l’ampia panoramica derivante dalla revisione della letteratura evidenzia esiti di maggiore benessere psicologico, aumentate abilità metacognitive e potenziate capacità cognitive dopo interventi psicologici e psicoterapici in particolare con soggetti con disturbi cognitivi soggettivi (Bhome et al., 2018).
Particolare attenzione è stata rivolta alle abilità metacognitive poiché tali capacità sembrano ridotte nei soggetti con SCD rispetto a persone che non lamentano e non manifestano difficoltà cognitive. Siamo oggi a conoscenza del fatto che la presa in carico psicologica di persone con SCD, in particolare attraverso interventi psicoeducativi di gruppo, abbia promosso una riduzione dei sintomi percepiti e un riferito miglioramento della qualità della vita (si veda la revisione di Bhome et al, 2018). Tale dato potrebbe essere spiegato dal potere benefico del ‘cambiamento di aspettativa’ che nello specifico interventi psicoeducativi e di ristrutturazione cognitiva sembrano favorire unitamente all’empowerment metacognitivo. Tali interventi hanno infatti la finalità di promuovere nei pazienti nuovi modi, più funzionali e adattivi, di reagire e di pensare rispetto alle proprie competenze cognitive ed emotive.
Un’attenta revisione della letteratura, a cura di Bhome e collaboratori (2018), ci fornisce una panoramica degli interventi psicologici, diretti in particolare alle persone con SCD, e alla rispettiva efficacia in termini di rilevazione dei principali output. La sintesi di questa revisione propone l’importanza del supporto psicologico, anche attraverso interventi di psicoeducazione e di empowerment cognitivo, al fine di favorire un maggiore benessere psicologico e un miglioramento della metacognizione che ha di conseguenza impatto benefico sulla percepita riduzione delle difficoltà cognitive. Tuttavia, è doveroso denunciare la mancanza di studi di elevata qualità. Gli studi oggi reperibili presentano dati relativi a campioni non sufficientemente numerosi per avere risultati solidi, ma ciò che è evidente e certa è la potenzialità di questi interventi. Si tratta sicuramente di una direzione promettente. È ancora limitata invece la ricerca nei confronti degli interventi sullo stile di vita e non sono convincenti in termini statistici e di qualità le prove relative agli interventi farmacologici e complementari nelle persone con SCD.
Anche la letteratura relativa al MCI e agli interventi non farmacologici di presa in carico ci fornisce dati interessanti. Seppur esista un maggior numero di studi rispetto alla condizione di SCD, anche qui non godiamo di studi con evidenze statisticamente forti. Tuttavia, pare essere pensiero condiviso che le persone con MCI presentino spesso, soprattutto in fase iniziale, sintomi quali ansia e depressione. Disturbi d’ansia e dell’umore possono avere un impatto sostanziale sulla qualità della vita della persona con MCI poiché sembrano correlati all’aumento del rischio di maggiore perdita di indipendenza e di maggiore distress del caregiver. La letteratura evidenzia inoltre che nell’MCI i sintomi depressivi precoci possono essere spesso resistenti alla terapia farmacologica.
Gli interventi psicologici basati su approcci e orientamenti diversi come da criteri dell’OMS (counselling psicologico, Cognitive-Behavior Therapy e approcci interpersonali) sono stati associati a effetti statisticamente positivi nella riduzione della sintomatologia depressiva oltre che degli stati d’ansia, seppur con minore evidenza per quest’ultima. Tenendo ovviamente in considerazione la rilevazione oggettiva di un deficit cognitivo, che guida l’équipe curante nella proposta di interventi farmacologici e non, la persona con SCD e con MCI ha il diritto di essere presa in cura, prima che in carico, in modo globale e multiprofessionale. In particolare, si ritiene urgente una presa in cura che passa dall’accompagnamento della persona attraverso interventi psicologici di supporto e di psicoeducazione, oltre che di empowerment cognitivo, alla luce delle evidenze di efficacia nella popolazione anziana (Orgeta et al., 2015).
È fondamentale quindi continuare ad interrogarci sui modi in cui, oggi, siamo curati quando ci ammaliamo. Ci sono norme etiche che regolano il rispetto della dignità umana, il riconoscimento del valore della persona e il diritto alla autodeterminazione. La presa in cura passa dall’accompagnare la persona che lamenta fatiche nuove, e/o che riceve una diagnosi, e la sua famiglia in un percorso durante il quale non c’è il tempo dell’adattamento ai continui cambiamenti. Ma ancora più importante resta il riconoscimento della dignità del vero protagonista della sua storia: la persona.
Conclusioni
Un cambio di prospettiva. Un diverso orientamento che ci porta a riconoscere la necessità di passare dalla logica del curare il malato, alla logica del prenderci cura della persona. Persona che ha bisogno di riconoscimento, di comunicazione e di accompagnamento. Riteniamo fondamentale che, come il Piano Nazionale Demenze sottolinea in diversi punti, la cura alla persona con SCD, MCI e demenza debba essere progettata precocemente e simultaneamente a partire dal reale incontro e scambio tra le diverse figure professionali che fanno parte dell’équipe di cura. Solo un effettivo e puntuale confronto tra tutti i professionisti dell’équipe curante, oltre al reciproco riconoscimento, potrà portare all’attivazione degli interventi di cura in cui i bisogni della persona siano realmente al centro.
Foto di Myriam Zilles da Pixabay
- La teoria del “gap” di Calman ha un ruolo di rilievo all’interno dei contributi alla delineazione del concetto di Qualità di Vita, in particolare in ambito oncologico. Secondo l’autore la QdV è identificabile con l’entità della distanza tra le aspettative e la realtà della persona. Più questi due elementi sono distanti, peggiore sarà la QdV percepita dalla persona (Calman, 1984)
NOTE
BIBLIOGRAFIA
Begum A., Morgan C., Chiu C-C., Tylee A., Stewart R., (2012), Subjective memory impairment in older adults: aetiology, salience and help seeking, in International Journal of Geriatric Psychiatry, Jun; 27(6), 616-620.
Bhome R., Berry A.J., Huntley J.D., Howard R.J., (2018), Interventions for subjective cognitive decline: systematic review and meta-analysis, in BMJ Open, Jul; 19, 8(7).
Borgia E., (2013), La dignità ferita, Edizioni Feltrinelli, Milano.
Calman KC., (1984), Quality of life in cancer patients – an hypothesis, in Journal of Medical Ethics, Sep; 10(3), 124-127.
Hessen E., Eckerström M., Nordlund A., Almdahl I.S., Stålhammar J., Bjerke M., Eckerström C., Göthlin M., Fladby T., Reinvang I. and Wallin A., (2017), Subjective cognitive impairment is a predominantly benign condition in memory clinic patients followed for 6 years: The Gothenburg-Oslo MCI study, in Dementia and Geriatric Cognitive Disorders, Jan-Apr 2; 7(1), 1-14.
Jessen F., Amariglio R.E., van Boxtel M., Breteler M., Ceccaldi M., Chételat G., et al. (2014), A conceptual framework for research on subjective cognitive decline in preclinical Alzheimer’s disease, in The Journal of Alzheimer’s Association, Nov; 10(6), 844-852.
Mitchell A.J., Beaumont H., Ferguson D., Yadegarfar M., Stubbs B., (2014), Risk of dementia and mild cognitive impairment in older people with subjective memory complaints: meta-analysis, in Acta Psychiatr Scand, Dec; 130(6), 439-451.
Orgeta V, Qazi A, Spector A, Orrell M., (2015), Psychological treatments for depression and anxiety in dementia and mild cognitive impairment: systematic review and meta-analysis, in The British Journal of Psychiatry: the Journal of Mental Science, Oct; 207(4), 293-298.
Petersen R.C., Smith G., Waring S., Invik R., Tangalos E. and Kokmen E., (1999), Mild Cognitive Impairment: clinical characterization and outcome, in Archives of Neurology, Mar; 56(3), 303-308.
Petersen R.C., Caracciolo B., Brayne C., Gauthier S., Jelic V., Fratiglioni L., (2014), Mild cognitive impairment: a concept in evolution, in Journal of Internal Medicine, Mar; 275(3),214-228.
Petersen R.C., Lopez O., Armstrong M.J., Getchius T.S.D., Ganguli M., Gloss D., et al., (2018), Practice guideline update summary: Mild cognitive impairment: Report of the Guideline Development, Dissemination, and Implementation Subcommittee of the American Academy of Neurology, in Neurology, Jan; 16,90(3), 126-135.
Waldorff F.B, Rishoj S., Waldemar G., (2008), If you don’t ask (about memory), they probably won’t tell, in J Fam Pract, 57:41-44.