
Premessa
La demenza costituisce una delle emergenze sanitarie che oggi i Paesi si trovano ad affrontare e, in futuro, assumerà dimensioni ancora più drammatiche a causa dell’invecchiamento delle popolazioni. L’incremento mondiale di ultrasessantenni previsto tra il 1990 e il 2030 è del 180%, con un aumento in valore assoluto da 488 milioni a 1,3 miliardi (World Bank, 1993). Considerato che sia l’incidenza sia la prevalenza della demenza aumentano con l’avanzare dell’età, il rapido aumento dei segmenti più vecchi della popolazione comporterà inevitabilmente un incremento delle malattie associate all’età, come risultato del semplice andamento demografico (Trabucchi, 2005).
La demenza è una malattia di lunga durata e altamente invalidante. Dall’esordio dei sintomi alla morte la persona affetta da demenza passa dalla completa autosufficienza alla totale dipendenza, dalla piena capacità di autodeterminazione alla assoluta incompetenza cognitiva. Questo processo avviene gradualmente, risulta progressivo e in larga misura imprevedibile, essendo condizionato dal tipo di demenza, dall’età, dalla comorbidità, dagli interventi sanitari assistenziali e dalla rete sociale (McClendon et al., 2004). L’assistenza all’anziano con deterioramento cognitivo rappresenta uno dei problemi più impegnativi che oggi possano presentarsi. La maggior parte dei pazienti dementi (circa l’80%) vive per molti anni in famiglia (Bianchetti e Zanetti, 1991) e i due terzi dei pazienti affetti da malattia di Alzheimer sono assistiti da familiari e amici, di cui il 70% è rappresentato da donne, per lo piú coetanee.
Nelle fasi avanzate della malattia il ricovero in istituti per anziani è molto frequente. Gli ultimi periodi di vita sono trascorsi, nella maggioranza dei casi, in istituzione (RSA), e quindi le cure di fine vita vengono per lo più erogate in questo ambito (Office of technology assessment, 1987; Temkin-Greener e Mukamel, 2002). In Italia non esistono dati relativi al tipo di cure a cui vengono sottoposte le persone affette da demenza severa nell’ultima fase della loro esistenza: in particolare, non è noto se il tipo di approccio sia prevalentemente interventista o palliativista. I problemi nella gestione del dolore, dell’alimentazione, dell’idratazione artificiale, della rianimazione, della contenzione, dell’uso di antibiotici, delle trasfusioni e della dialisi sono aspetti in comune a tutti i malati terminali.
Nella specifica ottica del paziente affetto da demenza, il quadro risulta ulteriormente complicato per due ordini di motivi: il primo è l’incompetenza cognitiva del malato, e quindi la necessità di operare scelte per conto dell’interessato, con le implicazioni di ordine morale, etico e medico-legale che ne derivano. Il secondo aspetto specifico della demenza è l’imprevedibilità del decorso, che rende difficoltosa la definizione temporale del concetto di “terminalità” e l’aspettativa di vita (Mitchell et al., 2004b). I pochi dati disponibili dalla letteratura suggeriscono che le persone affette da demenza all’ultimo stadio della malattia, ricoverate in RSA, non siano percepite come terminali, non ricevano cure palliative ottimali e che sia quindi necessario un rilevante intervento educativo nei confronti degli operatori che si occupano di demenza grave (Van der Steen et al., 2004; SomogyiZalud et al., 2002; Morrison e Siu, 2000).
Se le RSA continueranno a provvedere alle cure di fine vita, occorrerà focalizzare l’assistenza sulle aspettative degli ospiti e della famiglia, garantendo un’elevata soddisfazione nella cura. Conoscere i sintomi e i disordini percepiti dai pazienti che vivono nelle RSA durante la fase terminale della malattia, può aiutare a migliorare la qualità della presa in carico della fase terminale (Mitchell et al., 2004a). Questo studio replica un lavoro condotto in alcune RSA della provincia di Cremona (Toscani et al., 2008).
Obiettivi
- Quantificare il numero di pazienti deceduti con diagnosi di Demenza grave nelle RSA.
- Descrivere l’ultimo mese di vita in base ai dati ricavati dalle cartelle cliniche ed infermieristiche, con particolare attenzione alle condizioni generali, all’uso dei farmaci, a trattamenti ed interventi eseguiti, dal tipo di presa in carico, dall’incidenza di eventi critici, dalla presenza di sintomi e problemi importanti ed eventuali decisioni di fine vita.
Materiali e metodi
È stato condotto uno studio retrospettivo sui pazienti deceduti nei 12 mesi precedenti in 9 RSA dell’area torinese. I dati sono stati raccolti dalle cartelle cliniche e, dove disponibili, infermieristiche, su tutti i pazienti deceduti con diagnosi di demenza grave (demenza, Alzheimer, demenza vascolare o gravi alterazioni cognitive), e stadio FAST >7C (Sclan e Reisberg, 1992), degenti nella RSA da almeno un mese e che non avessero subito ricoveri prolungati nel mese precedente il decesso.
La Scala FAST, specifica per i pazienti con Alzheimer, è composta da 7 stadi per un totale di 16 stadi e sottostadi, da 1 a 7 (lo stadio 7 indica uno stadio di demenza avanzato: un paziente in stadio 7 ha limitazioni del linguaggio; nello stadio 7F non riesce a tenere la testa sollevata). La raccolta dati è stata effettuata da almeno 2 rilevatori addestrati in modo da uniformare le modalità di rilevazione e di evitare bias di interpretazione. Eventuali discrepanze sono state risolte con la discussione. Per ciascuna struttura sono stati raccolti alcuni dati essenziali che ne consentano la descrizione. Per identificare i pazienti eleggibili sono state consultate tutte le cartelle cliniche dei pazienti deceduti, identificate quelle dei pazienti con diagnosi di demenza e valutate per i criteri di eleggibilità. Sono stati rilevati i punteggi del Short Portable Mental Status Questionnaire (Pfeiffer, 1975) ed il punteggio FAST è stato ricavato dalle informazioni presenti in cartella.
Sono stati raccolti i seguenti dati: a. ultimi 30 giorni di vita: malattie concomitanti, segni e sintomi e loro intensità (grave-non grave) e incidenza (presente per una settimana/più di una settimana), lesioni da decubito, trattamenti (antibiotici, analgesici-scala analgesica dell’OMS (Ventafridda et al., 1987), ansiolitici, antidepressivi, nutrizione/idratazione artificiale, procedure chirurgiche, uso di mezzi di contenzione, trasferimento in ospedale. b. le ultime 48 ore di vita: rianimazione cardiopolmonare, tentativi di rianimazione e somministrazione di farmaci salvavita. È stato segnalato, anche se documentato, il coinvolgimento dei familiari nelle decisioni di fine vita.
Privacy
Non sono stati raccolti dati sensibili sui pazienti. Le schede, anonime, non consentono né di identificare il paziente né di associare le informazioni raccolte con i pazienti. L’associazione tra identità del paziente e scheda di raccolta dati è stata fatta su un registro rimasto all’interno della struttura e sarà distrutto al termine dello studio. I dati sono stati analizzati cumulativamente, senza fare riferimento al singolo paziente deceduto.
Risultati
Le 9 RSA coinvolte nello studio dispongono di un totale di 1.070 posti letto, e 4 nuclei per persone con malattia di Alzheimer. Sono state esaminate 345 cartelle cliniche. Il numero dei ricoveri, nell’anno solare preso in esame, varia da 16 a 65 (media 39,5 ricoveri).
Su 345 decessi, gli eleggibili sono risultati 71. I principali dati sui pazienti sono riportati nella Tabella 1.

Non sempre è stato possibile risalire alle cause di morte perché in più di un quarto delle cartelle esaminate non era riportata la diagnosi di morte. I sintomi del paziente nel mese precedente il decesso sono riportati nella Tabella 2.
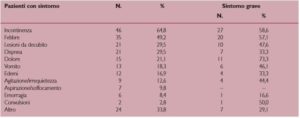
Nel mese precedente il decesso 27 pazienti (38%) provano sintomi gravi. Data la tipologia di problemi che si verificano in questo tipo di pazienti (inalazione di alimenti, allettamento, incontinenza con cateterizzazione, e infezioni del tratto urinario e polmonari) la febbre è il problema più riportato. Circa il 30% dei pazienti ha dispnea. È inaspettatamente basso il numero di pazienti con dolore e con convulsioni. Alla maggioranza dei pazienti con dolore (11/15) vengono somministrati analgesici, somministrati però anche a 5 pazienti per i quali non era segnalato dolore in cartella.
Complessivamente, 16 pazienti assumono analgesici: 5 oppioidi forti (gradino 3 della scala dell’OMS), 4 su base regolare; 2 oppioidi deboli (gradino 2 della scala dell’OMS), di cui uno su base regolare. Complessivamente viene trattato con analgesici il 22.5% dei pazienti. Nell’ultimo mese di vita, 37 pazienti (52,1%) hanno avuto un trattamento con antibiotici, 16 con tranquillanti (22,5%), 3 (4,2%) con antidepressivi. Dei pazienti a cui sono stati somministrati ansiolitici, per 6 in cartella veniva segnalata agitazione. In 5 casi il paziente viene alimentato artificialmente con PEG (per uno, impostata 90 gg prima del decesso) ed in un caso con SNG. Più elevato il ricorso all’idratazione: 47 pazienti (61,9%) vengono idratati artificialmente: 8 con ipodermoclisi e 34 per via endovenosa (per gli altri la via non era specificata). La durata della terapia endovenosa varia da 1 a 59 gg (mediana 12). In 20 casi non è stato possibile rilevare il dato per la mancanza di informazioni in cartella. La pratica dell’idratazione artificiale è egualmente diffusa in tutte le RSA. Solo un paziente viene ricoverato in ospedale per interventi chirurgici. Cinquantacinque pazienti vengono contenuti con le spondine al letto (in 15 casi per motivi di sicurezza).
In due RSA venivano contenuti con le spondine tutti i pazienti, nelle altre veniva segnalato sporadicamente. Solo in 5 casi viene segnalata la contenzione degli arti superiori ed in un caso l’uso della cintura addominale, sempre per motivi di sicurezza. Al momento della morte due pazienti vengono sottoposti a trattamenti rianimatori. Per 10 pazienti sono stati attuati interventi e terapie d’urgenza. Infatti 10 ricevono farmaci salvavita, 7 ossigenoterapia, 4 prelievi ematici, 3 ECG, 1 viene sottoposto a broncoaspirazione e 2 ad altri interventi. I numeri sono molto esigui ma il ricorso a farmaci salvavita è concentrato in 4 RSA. Non sono documentate in cartella direttive anticipate, ed il coinvolgimento della famiglia viene documentato in due sole occasioni.
Discussione
Lo studio descrive l’ultimo mese di vita nei pazienti con demenza grave ricoverati in RSA. La popolazione in studio è molto anziana e le patologie concomitanti rispecchiano quelle di pazienti con demenza in altri studi (Brandt et al., 2005; Evers et al., 2002).
La qualità delle cartelle cliniche non era ottimale, infatti la causa di morte non è stata riportata per il 28% dei pazienti. A differenza dello studio di Brandt et al. (2005), dove i principali sintomi erano debolezza generalizzata, problemi respiratori e sonnolenza e febbre, i principali sintomi/problemi riportati sono incontinenza, febbre, dispnea, lesioni da decubito. Altri sintomi comuni quali astenia o sopore sono stati riportati in pochissimi casi, probabilmente perché considerati caratteristiche della malattia, e pertanto situazioni attese.
In 3 RSA per nessuno dei pazienti deceduti viene segnalato dolore, difficile da rilevare in questi pazienti, soprattutto in assenza di strumenti specifici di valutazione (Sentagen e King, 1993). Quando il dolore viene segnalato, il paziente viene trattato con analgesici. Ci sono pochi dati sulla prevalenza di convulsioni (Mendez e Lim, 2003), ma la segnalazione di due soli casi sembra bassa. Probabilmente, il fatto di aver limitato l’osservazione all’ultimo mese di vita ha avuto come conseguenza una minor segnalazione di alcuni sintomi. Non sono stati raccolti i dati sui motivi per i quali vengono prescritti ansiolitici ed antidepressivi: naturalmente la prescrizione dipende dalle condizioni del paziente, anche se è difficile giustificarla in pazienti in fase di demenza così avanzata. Il numero di pazienti con lesioni da decubito è abbastanza alto e paragonabile a quanto rilevato in altre RSA (Toscani et al., 2008). Mitchell et al. (2004a) hanno riportato che il 35% dei pazienti con demenza grave aveva lesioni da decubito. Anche se le lesioni potrebbero essere considerate un fenomeno scarsamente prevenibile in pazienti allettati, incontinenti, contenuti, la elevata prevalenza è preoccupante e richiederebbe interventi specifici.
Nell’ultimo mese di vita vengono segnalati interventi che potrebbero essere definiti inappropriati per un paziente in fase terminale (Ahronheim et al., 1996), in particolare l’alimentazione e l’idratazione per via endovenosa. Il ricorso all’alimentazione artificiale è molto limitato rispetto ai dati di contesti internazionali (Monteleoni e Clark, 2004; Mitchell et al., 2003). L’uso di antibiotici (52%) è in linea con quanto riportato in altri studi su pazienti in fase terminale (Mitchell et al., 2004a) e più basso rispetto a quanto rilevato nelle RSA della provincia di Cremona (73%, Toscani et al., 2008): non è possibile in base ai dati di questo studio esprimere alcuna valutazione di appropriatezza.
Le spondine vengono utilizzate sempre per la maggioranza dei pazienti: molto limitato, invece, il ricorso ad altre forme di contenzione, e probabilmente determinato dalla necessità di immobilizzare gli arti per la terapia endovenosa (Toscani et al., 2008). Non ci sono studi che descrivano l’uso dei mezzi di contenzione su pazienti in fase terminale: studi che valutano l’efficacia degli interventi formativi per la riduzione dell’uso della contenzione indicano che prima degli interventi formativi viene contenuto fino al 70% dei pazienti (Testad et al., 2005).
Il ricorso a mezzi di contenzione chimici e fisici potrebbe indicare una cattiva gestione del dolore (che molti pazienti manifestano con agitazione) o mancanza di personale. Solo pochi pazienti vengono sottoposti a interventi salvavita o pratiche rianimatorie. Non è semplice fare un commento sull’appropriatezza della gestione dei pazienti perché dipende da numerosi fattori: l’organizzazione, i desideri dei parenti, la cultura locale. In ogni caso, il coinvolgimento dei parenti sembra essere l’eccezione: non solo le decisioni dovrebbero essere condivise con i parenti, ma devono essere anche registrate in cartella clinica. Nonostante la prevalenza di alcuni trattamenti sia inferiore rispetto a quanto riportato in altri studi (Brandt et al., 2005; Testad et al., 2005; Moss et al., 2002) la responsabilità di introdurre nelle RSA una maggiore attenzione alle cure palliative non può essere responsabilità dei soli medici ed infermieri: occorre il coinvolgimento della famiglia e vanno trovati sistemi per raccogliere e tenere conto delle indicazioni/desideri dei pazienti. La scarsità di dati di confronto italiani (e, in generale, nel contesto internazionale) sottolinea la necessità che le RSA diventino sempre di più un luogo di ricerca (Mitchell et al., 2006).

Limiti dello studio
I dati sono stati raccolti nell’ultimo mese di vita, ma non esiste un consenso sulla durata della fase terminale in questi pazienti, ed è possibile che alcune decisioni critiche siano già state prese. Solo raramente sulle cartelle ne vengono riportate le motivazioni.
Ringraziamenti
Si ringraziano i responsabili delle seguenti RSA Torinesi: Istituto Carlo Alberto, Istituto di Riposo per la vecchiaia, Residenza “Le Terrazze”, Residenza “5 Torri”, Residenza per gli anziani “Anni Azzurri”, Convitto Principessa Felicita di Savoia, RSA “A. Ballestrero”, Senior Residence e Residenza Principe Oddone per aver messo a disposizione i dati per lo studio.
Questo studio è stato possibile grazie al finanziamento Progetti di Ricerca Finalizzata della Regione Piemonte (Bando 2004).
Bibliografia
Ahronheim JC, Morrison RS, Baskin SA, Morris J, Meier DE. Treatment of dying in the acute care hospital. Advanced dementia and metastatic cancer. Arch Intern Med 1996;156:2094-100.
Bianchetti A, Zanetti O. Dipartimento di ricerca clinica per la Malattia di Alzheimer: una risposta ai problemi della demenza. Psichiatria Oggi 1991; 4:94.
Brandt HE, Deliens L, Ooms ME, van der Steen JT, van der Wal G, Ribbe MW. Symptoms, signs, problems, and diseases of terminally ill nursing home patients: a nation-wide observational study in the Netherlands. Arch Intern Med 2005:165:314-20.
Evers MM, Purohit D, Perl D, Khan K, Marin DB. Palliative and aggressive end-of-life care for patients with dementia. Psychiatric Services 2002;53: 609-13.
McClendon MJ, Smyth KA, Neundorfer MM. Survival of persons with Alzheimer disease: caregiver coping matters. Gerontologist 2004;44(4):508-19.
Mendez M, Lim G. Seizures in elderly patients with dementia: epidemiology and management. Drugs Aging 2003;20:791-803.
Mitchell SL, Kiely DK, Hamel BH. Dying with advanced dementia in the nursing home. Arch Intern Med, 2004a 164:321-326.
Mitchell SL, Kiely DK, Hamel MB, Pak PS, Morris JN, Fries BE. Estimating prognosis for Nursing Home residents with advanced dementia. JAMA, 2004b;291:2734-40.
Mitchell SL, Kiely DK, Jones RN, Prigerson H, Volicer L, Teno JM. Advanced dementia research in the nursing home: the cascade study. Alzheimer Dis Assoc Disord 2006;20:166-75.
Mitchell SL, Teno JM, Roy J, Kabumoto G, Mor V. Clinical and organizational factors associated with feeding tube use among nursing home residents with advanced cognitive impairment JAMA 2003;290:73-80.
Morrison RS, Siu A. Survival in end-staged dementia following acute illness. JAMA 2000;284:47-52.
Monteleoni C, Clark E. Using rapid-cycle quality improvement methodology to reduce feeding tubes in patients with advanced dementia: before-after study. BMJ 2004;329:491-4.
Moss MS, Braunschweig H, Rubinstein RL. Terminal care for nursing home residents with dementia. Alzheimer’s Care Quart 2002;3:233-46.
Office of Technology Assessment. Losing a million minds: confronting the tragedy of Alzheimer’s disease and related dementias. Washington, US 1987. Pfeiffer E. A short portable mental status questionnaire for the assessment of organic brain deficit in elderly patients. J Am Ger Soc 1975;23(10):43341.
Sclan SG, Reisberg B. Functional assessment staging (FAST) in Alzheimer’s disease: reliability, validity, and ordinality. Int Psychogeriatr 1992;4 Suppl 1:55-69.
Sentagen EA, King SA. The problems of pain and its detection among geriatric nursing home residents. J Am Ger Soc 1993;41(5):541-4.
Somogyi-Zalud E, Zhong Z, Hamel MB, Lynn J. The use of life sustaining treatments in hospitalized persons aged 80 and older. J Am Ger Soc 2002; 50:930-4.
Temkin-Greener H, Mukamel DB. Predicting place of death in the program of All-Inclusive Care for Ederly (PACE): participant versus program characteristics. J Am Ger Soc 2002;50:125-35.
Testad I, Aasland AM, Aarsland D. The effect of staff training on the use of restraints in dementia: a single-blind randomised controlled trial. J Geriatr Psychiatry 2005;20:587-90.
Toscani F, Di Giulio P, Villani D, Brunelli C, Gentile S, Spadin P. Dying with advanced dementia in long-term care geriatric institutions: a retrospective study. Accepted J Pall Care, 2008.
Trabucchi M. Le demenze. IV edizione. UTET Ed. Torino 2005:13-19.
Van der Steen JT, Kruse RL, Ooms ME, Ribbe MW, van der Wal G, Heintz LL, Mehr D. Treatment of Nursing Home residents with dementia and lower respiratory tract infection in the United States and Netherlands: an ocean apart. J Am Ger Soc 2004;52:691-9.
Ventafridda V, Tamburini M, Caraceni A et al. A validation study of the WHO method for cancer pain relief. Cancer 1987;59:851-6.
World Bank. World Development Report 1993. New York, Oxford University Press, 1993.













