
Introduzione
Il significato ed il ruolo della riabilitazione geriatrica sono ancora oggi una vexata quaestio. Innanzitutto vi è chi sostiene che con il termine “riabilitazione geriatrica” si intende un insieme di attività troppo eterogenee e non confrontabili, tra le quali alcune sembrano eccessivamente distanti da un modello di riabilitazione classicamente inteso. Si pensi, ad esempio, al fatto che questa disciplina non trovi ancora oggi una collocazione precisa per quanto concerne il setting in cui debba essere effettuata (se cioè debba essere praticata all’interno di ospedali, in strutture extraospedaliere o ancora possa essere praticata anche nelle case di riposo) ed anche al problema della “post-acuzie” che, nonostante il fiorire di interessi sulle cure intermedie, appare un’entità non ben definita e lungi dal trovare una sistematizzazione.
Un secondo motivo è di carattere più squisitamente pratico. Fino a qualche anno fa pensare di sottoporre ad un trattamento riabilitativo un paziente anziano era considerato dagli addetti ai lavori quasi un non-sense, una contraddizione in termini. Il paziente anziano, non sempre in grado di collaborare al trattamento fisioterapico proposto e di tollerare carichi intensivi di lavoro, era considerato non eleggibile al trattamento stesso e di fatto aprioristicamente escluso da qualsiasi attività riabilitativa. Oggi, fortunatamente, l’attenzione nei confronti del paziente anziano e delle problematiche cliniche e gestionali correlate all’invecchiamento è decisamente aumentata, sebbene non si possa fare a meno di osservare che esistano ancora sacche di pregiudizio culturale in varie parti della nostra penisola.
Perché sono necessari i reparti di riabilitazione geriatrica?
Negli ultimi anni, l’epidemiologia dei bisogni è profondamente cambiata anche in ambito riabilitativo. A questo cambiamento hanno certamente contribuito i grandi sovvertimenti demografici degli ultimi anni, caratterizzati da una crescita esponenziale dell’età media della popolazione e da una compressione della disabilità verso le fasce di età più elevate.
I dati ISTAT dell’ultimo quinquennio, a supporto di queste osservazioni dimostrano, ad esempio, che il 72% degli ictus si verifica in persone anziane e che oltre l’80% delle fratture registrate nei soggetti di sesso femminile si verifica in donne ultra-settantacinquenni (Rossini et al., 2005). Nello specifico, l’aumento del numero di ricoveri per frattura femorale osservato nel quadriennio 1999-2002 sembra essere quasi esclusivamente attribuibile all’incremento del numero di fratture verificatesi nelle donne di età superiore ai 75 anni, che sono passate da 47.552 (1999) a 53.628 (2002), con un incremento dell’11.3% in 4 anni (Rossini et al., 2005). Nello stesso periodo, i ricoveri per frattura femorale nel sesso maschile sono passati da 11.702 a 13.582 (Rossini et al., 2005).
La Tabella 1 mostra l’evoluzione delle caratteristiche degli utenti di un reparto di riabilitazione geriatrica negli anni dal 2003 al 2007.

I dati indicano un significativo aggravamento delle condizioni cliniche, cognitive e funzionali, evidenziando indirettamente la tendenza (sia pure con tutti i limiti dell’estrapolazione) a ricoverare persone nelle quali la relazione tra disabilità motoria (Barthel Index), disabilità cognitiva (Mini Mental State Examination), comorbidità (Charlson Index) e fragilità (numero di eventi avversi occorsi durante la degenza) è molto stretta. Tale osservazione sembra essere supportata anche da recenti reviews, secondo le quali – sebbene siano da considerarsi condizioni distinte – disabilità, fragilità e comorbilità sono in realtà molto spesso interagenti e coesistenti (Fried et al., 2001; Fried et al., 2004).
Datidel Women’s Health and Aging Study (Xue et al., 2008) indicano che circa il 30% dei soggetti moderatamente o gravemente disabili è contemporaneamente anche fragile e con polipatologia. Un ulteriore elemento di complessità, che ha caratterizzato l’utenza dei reparti di riabilitazione geriatrica negli ultimi anni, è dato dall’instabilità clinica e dagli scompensi. L’instabilità clinica è una dimensione tradizionalmente considerata soltanto in medicina per acuti ma che, invece, è oggi rilevante da un punto di vista epidemiologico anche in riabilitazione. A questo proposito, un recente articolo pubblicato su JAMA (Ottenbacher et al., 2004) ha chiaramente mostrato che negli Stati Uniti, dal 1994 al 2001, il numero degli utenti ricoverati in reparti di riabilitazione ospedaliera con problematiche di instabilità clinica è significativamente aumentato tanto che, a fronte di una maggiore efficacia (incremento del punteggio alla scala FIM) ed efficienza (incremento del punteggio FIM/durata della degenza) degli interventi, è aumentato in modo proporzionale anche il tasso di mortalità durante la degenza.
Anche in Italia, seppure manchino dati così precisi, lo scenario non è granché differente. L’introduzione di un nuovo sistema di remunerazione delle tariffe di degenza e la pressione esercitata dagli ospedali per una rapida dimissione (in ragione dei DRG che incentivano a contenere le durate della degenza), hanno finito con il favorire i trasferimenti sempre più frequenti di pazienti ancora instabili, o non perfettamente compensati sotto il profilo clinico, verso strutture di riabilitazione, che dunque oggi devono fare i conti con un’utenza significativamente differente da quella che era ricoverata nelle stesse strutture soltanto alcuni anni orsono. In questo contesto, la scelta degli interventi appropriati ed efficaci è una questione sempre più rilevante: l’efficacia delle cure prestate è infatti necessaria in uno scenario complessivo di contrazione delle risorse, onde evitare sprechi o soluzioni semplicistiche. L’ambito della riabilitazione geriatrica non si colloca al di fuori di questa problematica, ma anzi, ne è decisamente interessato.
Il modello della rehabilitation and Aged Care Unit
In un recente articolo pubblicato sugli Archives of Physical Medicine and Rehabilitation, Robert Kane afferma che nella riabilitazione delle persone anziane è difficile separare la fase di recupero spontaneo da quella di recupero dovuto ad un intervento riabilitativo specifico (Kane, 2007). In effetti è tipico osservare in questi pazienti miglioramenti significativi dello stato funzionale anche soltanto pochi giorni dopo l’inizio delle cure mediche ed infermieristiche. Dati di recente pubblicazione dimostrano, ad esempio, che la risoluzione del delirium (o stato confusionale acuto), ottenuta dopo aver instaurato cure mediche specifiche, permette evidenti miglioramenti dello stato funzionale in modo indipendente da una specifica attività fisioterapica (Speciale et al., 2007). Ad un’analisi sommaria, si potrebbe ritenere che il miglioramento funzionale così ottenuto dimostri indirettamente che in riabilitazione geriatrica l’intervento fisioterapico sia meno importante che in altri settori e che la dimensione clinico-assistenziale sia preponderante. Tale convinzione è erronea.
Come noto il delirium è unparadigma della complessità delle cure nel quale il lavoro d’équipe trova le basi per una riorganizzazione sistematizzata. A fianco dell’intervento del medico che deve saper riconoscere i fattori predisponenti e scatenanti il delirium, è fondamentale l’apporto dell’infermiere che individua e previene le possibili complicanze dell’allettamento e della sedazione, e del fisioterapista che legge il peggioramento/miglioramento della disabilità (e dunque dell’evoluzione clinica del delirium) nel paziente, prevenendo la comparsa di danni terziari (Bellelli et al., 2005). Quotidianamente, l’evoluzione clinica del paziente, misurata attraverso il riconoscimento della presenza/assenza del delirium, consentirà ad ogni membro dell’équipe di rivalutare il proprio assetto organizzativo, nello specifico del proprio ruolo ed in rapporto agli altri operatori (medici e non medici), nonché di modulare gli interventi di cura in modo armonico e coerente. In questa prospettiva il delirium, così come qualsiasi altra sindrome geriatrica, può essere “utilizzato” dall’equipe come luogo di collaborazione interdisciplinare e come modello prototipico di cura (Bellelli et al., 2005).
In un recente lavoro pubblicato sul Journal of American Medical Directors Association (Bellelli et al., 2008) è stato teorizzato il modello della Rehabilitation and Aged Care Unit (RACU). La RACU è un reparto dedicato alla cura di persone anziane disabili e fragili che propone un approccio operativo multiprofessionale e multimodale, in grado di coniugare interventi di tipo clinico, assistenziale, fisioterapico ed educativo-supportivo in un mix omogeneo ed efficace. La RACU, in qualche modo, si propone come prototipo di reparto di riabilitazione geriatrica, basandosi su alcune premesse di fondo che giustificano in chiave filosofico-organizzativa il modello che ne deriva. Un primo punto chiave è che la RACU accoglie tipicamente pazienti che, in aggiunta a problematiche riabilitative “pure” (cioè di disabilità acuta, cronica o mista), lamentano anche problemi di instabilità clinica e labilità dei compensi per quanto attiene allo stato di salute somatico. Un secondo punto chiave è che la RACU non prevede una distinzione formale tra riabilitazione intensiva ed estensiva, ma anzi favorisce la commistione nei medesimi reparti di pazienti con problematiche diverse. Ciò ha lo scopo primario di omogeneizzare gli ambienti di cura e favorire la nascita di modelli operativi in cui i pazienti possano trovare soddisfatti i propri bisogni non tanto sulla base di una maggior o minor intensità di trattamento (imposta da standard formali), quanto dall’effettiva valutazione dei bisogni assistenziali.
La Tabella 2 mostra le caratteristiche salienti di una popolazione di 1.300 pazienti ricoverati in RACU negli anni 2003-2007. Si tratta di pazienti con età media elevata (76.6 anni), prevalentemente di sesso femminile (72%), provenienti per circa la metà dei casi da ospedali per acuti (48%) e per l’altra metà dal domicilio (46%).
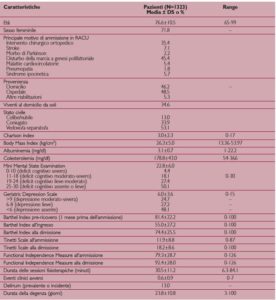
In genere il ricovero è motivato da problematiche ortopediche o neurologiche ancorché non siano state infrequenti malattie cardiocircolatorie e dell’apparato respiratorio. Poco più di un terzo di questi pazienti vive solo al proprio domicilio. In media il deficit cognitivo è di grado lieve (MMSE 22.8±6.0), sebbene circa un quinto dei pazienti mostri un decadimento di grado moderato-severo. Parimenti, circa un quarto dei pazienti ricoverati in RACU lamenta tono dell’umore moderatamente o severamente depresso. I pazienti appaiono in discrete condizioni nutrizionali, ancorché affetti da una comorbilità elevata (in media, 3.0±2.3 patologie con un elevato consumo di farmaci) e da una moderata compromissione funzionale per quanto concerne lo stato premorboso, l’ammissione in RACU e la dimissione. In media, circa un paziente su due sviluppa un evento clinico intercorrente durante la degenza in RACU (0.6±0.9 per paziente) e, tra questi, nel 13% dei casi si tratta di delirium (stato confusionale acuto). La degenza media è di poco superiore ai 23 giorni. Analizzando gli outcomes ad 1 anno dalla dimissione, si osserva una mortalità complessiva del 10.2%, un tasso di istituzionalizzazione dell’8.3% (3.3% alla dimissione e 5% nei successivi 12 mesi) ed un tasso di ospedalizzazione del 24%.
Tali risultati sono sorprendentemente migliori di quelli ottenuti in strutture riabilitative di oltreoceano, verosimilmente a causa del fatto che i pazienti statunitensi sono più gravi all’ammissione. Per ciascuno di questi outcomes è possibile individuare fattori predittivi differenti che permettano di pianificare un intervento assistenziale differenziato. Il rischio di istituzionalizzazione è ad esempio predetto dall’età elevata, dalla mancanza di supporto abitativo, dallo stato cognitivo e dalla presenza di delirium, nonché da una compromissione significativa dello stato funzionale. La presenza di delirium in associazione ad una comorbilità moderato-severa predice il rischio di ri-ospedalizzazione, mentre il decesso è predetto da un maggior numero di variabili (età, stato funzionale all’ammissione, comorbilità, depressione del tono dell’umore e bassi valori di albuminemia).
La valutazione degli outcomes in riabilitazione ed i modelli esistenti di attribuzione delle tariffe in riabilitazione. Alla ricerca di un sistema di classificazione iso-risorse ed outcom correlato
La valutazione degli outcomes è essenziale in riabilitazione sia per verificare la bontà dell’operato svolto ma anche in un’ottica di definizione del rapporto tra costi e benefici degli interventi. È infatti necessario un preciso sforzo da parte di chi ha la responsabilità dei servizi per definire i benefici ottenuti, altrimenti sarà difficile domandare alla generosità sociale di impegnarsi a favore dei pazienti più fragili. L’introduzione di linee guida secondo i principi dell’Evidence Based Medicine (EBM) ha certamente costituito una notevole spinta verso la definizione degli outcomes riabilitativi, anche se la loro costruzione si è dimostrata piena di incertezze e difficoltà legate a molteplici variabili (Trabucchi e Crepaldi, 2001; Tesio, 2007).
Innanzitutto va sottolineato che i risultati nel campo della riabilitazione geriatrica non sempre possono essere raggiunti in breve tempo, ed inoltre le linee guida possono essere molto utili per definire quale cura sia più appropriata, ma non possono certo sostituire il medico nella scelta dei tempi e dei modi della cura che, tanto più in un anziano, sarà articolata e varia. In questo scenario complesso, la creazione di sistemi di valutazione degli outcomes in riabilitazione ha comunque preso il via tra dubbi e perplessità, ed è diventata uno dei temi più “caldi” in ambito di programmazione della politica sanitaria. Non può infatti essere dimenticato che la possibilità di misurare gli outcomes riabilitativi in modo ordinato e finalizzato potrebbe consentire di addivenire a sistemi retributivi non più basati su criteri di processo o di standard strutturali, bensì sul raggiungimento di risultati.
Mediante sistemi retributivi di questo tipo si potrebbero ipotizzare maggiori retribuzioni per le strutture che abbiano dimostrato risultati migliori (ovviamente tarati sulla base della complessità clinica e riabilitativa) e, dunque, tendere ad un innalzamento consensuale del livello qualitativo atteso. Negli Stati Uniti, negli anni passati, sono state utilizzate numerose scale funzionali e misure di performances per la valutazione standardizzata dei pazienti in Post-Acute Care (PAC) (Keith et al., 1987; Moskowitz, 1985;TurnerStokes et al., 1999). Tra queste, la FIM™ è stata utilizzata per generare gruppi isorisorse attraverso una classificazione ed un approccio algoritmico “regression tree” (CART) (Keith et al., 1985), ed i FIM-FRG che ne conseguono sono stati utilizzati per il sistema di pagamento prospettico (Stineman et al., 1997; Stineman et al., 1994). Nel 1999-2000 il CMS (Center for Medicare and Medicaid Services), ex HCFA (Health Care Financing Administration) mise a punto uno strumento originale e molto dettagliato denominato Minimum Data Set-Post Acute Care (MDS-PAC), che venne testato in vari studi.
In aggiunta rispetto alla FIM™ il MDS-PAC conteneva informazioni accurate sul trattamento realmente effettuato, sulle modalità di gestione dei problemi e sulle condizioni cliniche dei pazienti. L’implementazione del MDS-PAC nei setting postacuti come strumento di assessment e come modalità di rimborso venne soppiantata nel 2002 dall’Inpatient Rehabilitation Facilities-Patient Assessment Instrument (IRFs-PAI), strumento più complesso che includeva la FIM™ quale misura di assessment funzionale.
In Italia il MDS-PAC è stato utilizzato in due studi finanziati dal Ministero della Sanità al termine dei quali si è dimostrata la possibilità di vincolare gli outcome al recupero funzionale, in particolare stimando adeguatamente i costi dell’intervento e determinando per ogni gruppo di malattia la durata della degenza ottimale per ottenere il recupero funzionale previsto (Saitto et al., 2005a; Saitto et al., 2005b). I due strumenti presentano vantaggi e svantaggi; il principale vantaggio è che tentano di correlare il pagamento all’outcome ottenuto alle risorse impiegate. Ciò è estremamente importante per favorire una crescita qualitativa del sistema riabilitazione, per premiare le strutture in grado di operare meglio e per evitare atteggiamenti opportunistici che potrebbero generarsi con un sistema tariffario fisso a giornata di degenza e soglia. Gli svantaggi sono legati essenzialmente alla complessità degli strumenti adottati ed al tempo richiesto per la compilazione (ad esempio l’MDS-PAC richiede misurazioni ad intervalli regolari nel corso della durata della degenza). Inoltre, l’uso di questi strumenti è stato validato utilizzando la variabile “durata della degenza” come parametro per misurare l’efficienza dell’intervento, e ciò sarebbe improponibile in Italia tenuto conto che la durata della degenza risente, come noto, di influenze legate alle condizioni sociodemografiche ed abitative dei pazienti. Tuttora negli Stati Uniti non è ancora condiviso un data-set standardizzato di outcomes “paziente centrati”, applicabile trasversalmente a differenti categorie diagnostiche e in setting di cura differenti, sufficientemente sensibile da cogliere i cambiamenti clinicamente significativi dello stato dei pazienti.
I percorsi clinici integrati (percorsi diagnostico terapeutici) e la loro mappatura
Se immaginiamo il processo riabilitativo come la pianificazione di una serie di interventi che accompagnano il paziente dalla fase acuta ospedaliera fino al rientro al domicilio e successivamente, nel medio-lungo periodo, attraverso i vari setting di cura, possiamo derivare un percorso clinico da organizzare attorno agli obiettivichiave della riabilitazione: la stabilizzazione clinica (compenso delle alterazioni fisiologiche legate alle malattie d’organo), il recupero funzionale (miglioramento delle limitazioni causate dalla malattia principale e dalla comorbilità e riduzione della disabilità), l’adattamento ambientale e socio-relazionale (rientro/mantenimento del paziente al domicilio o nel contesto di cura più appropriato). Questa complessa serie di interventi multiprofessionali deve inoltre salvaguardare il benessere psicologico e la qualità di vita del paziente stesso e dei suoi familiari (Bernardini et al., 2006).
Il metodo dei Percorsi Clinici Integrati (PCI) rappresenta un’evoluzione dell’approccio tradizionale alla valutazione dell’appropriatezza e dell’efficacia delle cure. I PCI sono algoritmi che definiscono formalmente i tempi e la sequenza delle attività diagnostico-terapeutiche programmate per la gestione di una determinata condizione patologica. Sebbene non vi siano ancora sufficienti prove di efficacia a supporto della loro applicazione nei pazienti con patologie complesse (ad esempio l’ictus o la frattura di femore nell’anziano vulnerabile), lo strumento dei PCI rappresenta lo standard organizzativo adottato da molte strutture per migliorare la qualità delle cure, ottimizzare l’uso delle risorse ed educare i componenti del team assistenziale.
I vantaggi principali offerti dal metodo dei PCI sono:
- l’aderenza al “mondo reale”: descrivono infatti le attività effettivamente svolte “rivelando” l’organizzazione interna del sistema di cura adottato, al di là dei parametri precostituiti dell’accreditamento;
- il focus sugli obiettivi: le attività diagnostico-terapeutiche sono finalizzate al raggiungimento di obiettivi (intermedi e finali) verificabili, che condizionano il percorso stesso e la sua evoluzione;
- l’enfasi sui processi di cura e la loro standardizzazione: la definizione e l’analisi della rete dei processi ne permette il controllo e una migliore pianificazione.
Una barriera che ostacola la progettazione di PCI in riabilitazione geriatrica è rappresentata dalla complessità del paziente anziano, che implica un disegno fortemente “paziente-dipendente”. Diversamente da altre patologie d’interesse riabilitativo per le quali sono stati sviluppati PCI (ad esempio interventi artroprotesi in elezione), nelle patologie complesse sono infatti le caratteristiche cliniche e funzionali del paziente che determinano le modalità dei trattamenti e la progressione del percorso. Il sistema IPER® (Bernardini et al., 2004), proposto da Bernardini e colleghi, è un sistema standardizzato di indicatori utilizzabile per la “macro-mappatura” del percorso di cura dei pazienti e la valutazione delle performance delle organizzazioni, almeno per i setting riabilitativi post-acuti (riabilitazione specialistica e generale geriatrica).
Il sistema origina direttamente dalle cartelle cliniche, valorizzando gli elementi considerati significativi dell’assessment multidimensionale e dei trattamenti effettuati, e permette l’analisi del case-mix dei pazienti trattati, della varietà ed entità dei processi di cura e degli obiettivi raggiunti. Il sistema è da considerare come una misura generica (generale) del percorso di cura dei pazienti, applicabile a qualsiasi condizione, indipendentemente dalla malattia principale che ha determinato il ricovero riabilitativo. Esso è basato su misure e strumenti validati, quali il Barthel Index modificato secondo Shah, la scala di Disabilità Comunicativa, il Mini Mental State Examination (MMSE), il Confusion Assessment Method (CAM), la Cumulative Illnesses Rating Scale (CIRS), e su misure standardizzate per identificare e/o stadiare specifiche condizioni come la malnutrizione, le ulcere da decubito, l’incontinenza urinaria.
Il core-set è composto da indicatori dicotomici (presenza o assenza della condizione target) scomponibile in quattro sottogruppi:
- Gli indicatori di stato focalizzano il profilo clinicofunzionale del paziente all’ammissione nell’unità di riabilitazione. Il subset è organizzato per evidenziare preesistenti fattori di rischio non modificabili (età ≥75 anni, comorbilità cronica, disabilità premorbosa, fragilità sociale) e fattori di rischio “emergenti” (modificabili): presenza di disabilità comunicativa, confusione, instabilità medica, malnutrizione, lesioni da pressione, catetere urinario, infezioni acute. Gli indicatori di stato, opportunamente trattati, possono essere utilizzati per stratificare il rischio dei pazienti di cattivi esiti clinici e funzionali.
- Gli indicatori di transizione misurano il profilo di cura del paziente per impegno medico e processichiave assistenziali. Identificano i pazienti che hanno necessitato di un workup diagnostico e di terapia mirata per eventi clinici avversi (infettivi e non infettivi), quelli caduti, che sono stati contenuti, o con necessità di trattamenti prolungati per il dolore, la depressione, la malnutrizione.
- Gli indicatori di esito organizzazione–orientati definiscono la allocazione dei pazienti alla dimissione dalla riabilitazione. Questi indicatori si escludono vicendevolmente: dimissione al domicilio senza necessità di ulteriore riabilitazione, prosieguo della riabilitazione con Assistenza Domiciliare Integrata, Day Hospital o altre strutture riabilitative, trasferimento in casa di riposo, trasferimento in unità di cura per acuti (per instabilità medica intrattabile), decesso (durante il decorso riabilitativo).
- Gli indicatori di esito paziente-orientati definiscono l’efficacia del trattamento riabilitativo per i pazienti sopravvissuti o non trasferiti in unità per acuti: indipendenza nel cammino, recupero funzionale completo, assenza di ulcere da pressione, catetere vescicale e continenza urinaria. Nella Figura 1 è riportata la scheda di raccolta degli indicatori. La compilazione della scheda, se basata su cartelle cliniche ben compilate, non richiede più di 10 minuti a paziente.

Conclusioni
Qualche tempo fa la geriatria era stata definita “una scienza non adatta ai deboli di cuore”. Si potrebbe estendere questa definizione anche alla riabilitazione geriatrica, per la complessità dei problemi clinici che deve affrontare (talvolta peraltro in ambienti di cura con limitate dotazioni tecnologiche), per le incertezze della prognosi, per le difficoltà organizzative tra interventi intensivi ed estensivi. Ma sono difficoltà che si affrontano e si superano con l’intelligenza della mente e la generosità del cuore, sapendo che attorno al tema riabilitazione-libertà ruotano molte attese e speranze nella vita degli anziani.
La geriatria è oggi pronta per recitare un ruolo importante nell’ambito della disciplina riabilitativa, non accontentandosi più di partecipare come comprimaria ai dibattiti sul tema, ma proponendosi come riferimento culturalmente adeguato ed attuale.
Bibliografia
Bellelli G, Pagani M, De Marco V, Trabucchi M. La cura del delirium: un luogo per la collaborazione tra medico ed infermiere. I luoghi della cura 2005; 4: 25-32.
Bellelli G, Magnifico F, Trabucchi M. Outcomes at 12 months in a population of elderly patients discharged from a rehabilitation unit. J Am Med Dir Assoc 2008; 9: 55-64.
Bernardini B, Bellelli G, Pagani M, Guaita A, (per il gruppo SIGG della Lombardia). Le basi metodologiche della cartella di riabilitazione geriatrica. I luoghi della cura 2006; 4: 19-25.
Bernardini B, Cappadonia C, Corsini C, Pagani M, Giardini S, Benvenuti F. Sistema IPER®: Indicatori di Processo-Esito in Riabilitazione. Vega Edizioni, Padova 2004.
Fried LP, Tangen CM, Waltson J et al. Frailty in older adults: evidence for a phenotype. J Gerontol A Biol Sci Med Sci 2001; 56: M134-5.
Fried LP, Ferrucci L, Dater J et al. Untangling the concepts of disability, frailty, and comorbidity: implications for improved targeting and care. J Gerontol A Biol Sci Med Sci 2004; 59A: 255-63.
ISTAT: dati reperibili sul sito web dell’ISTAT http://ionio.cineca.it/. Kane RL. Assessing the Effectiveness of Postacute Care Rehabilitation. Arch Phys Med Rehabil 2007; 88: 1500-4.
Keith RA, Granger C, Hamilton BB et al. The Functional Independence Measure: a new tool for rehabilitation. Adv Clin Rehabil 1987; 1: 6-16.
Keith RA, Breckenridge K.Characteristics of patients from the Hospital Utilization Project Data System: 1980-1982.
Arch Phys Med Rehabil 1985; 66: 768-72. Moskowitz
E. PULSES profile in retrospect. Arch Phys Med Rehabil 1985; 66: 647-8.
Ottenbacher KJ, Smith PM, Illig SB et al. Trends in length of stay, living setting, functional outcome, and mortality following medical rehabilitation. JAMA 2004; 292: 1687-95.
Rossini M, Piscitelli P, Fitto F et al. Incidenza e costi delle fratture di femore in Italia. Reumatismo, 2005; 57 (2): 97-102.
Saitto C, Marino C, Fusco D et al. Toward a new payment system for inpatient rehabilitation. Part I: predicting resource consumption. Med Care 2005a; 43: 844-55.
Saitto C, Marino C, Fusco D et al. Toward a new payment system for inpatient rehabilitation. Part II: Reimbursing providers. Med Care 200b; 43: 85664.
Speciale S, Bellelli G, Lucchi E, Trabucchi M. Delirium and functional recovery in elderly patients. J Gerontol A Biol Med Sci 2007; 62: 107-8.
Stineman MG, Tassoni CJ, Escarce JJ, et al. Development of function-related groups version 2.0: a classification system for medical rehabilitation. Health Serv Res 1997; 32: 529-48.
Stineman MG, Escarce JJ, Goin JE et al. A case-mix classification system for medical rehabilitation. Med Care 1994; 32: 366-79.
Tesio L. Functional assessment in rehabilitative medicine: principles and methods. Eura Medicophys 2007; 43: 515-23.
Trabucchi M, Crepaldi G. L’organizzazione dell’assistenza all’anziano: un puzzle con molti problemi aperti. In: Spalaore P, Maggi S, Trabucchi M (Eds). L’anziano nella rete dei servizi. Il Poligrafo, Padova 2001: 15-37.
Turner-Stokes L, Nyein K, Halliwell D. The Northwick Park Care Need Assessment (NPCNA): a directly costabel outcome measure in rehabilitation. Clin Rehabil 1999; 13: 253-67.
Xue QL, Fried LP, Glass TA et al. Life-space constriction, development of frailty, and the competing risk of mortality: the Women’s Health and Aging Study I. Am J Epidemiol 2008; 167: 240-8.













